该研究的次要重点是BIOTRONIK公司新型4F解决方案产品阵容优化结果的潜力
瑞士BUELACH--(美国商业资讯)--BIOTRONIK公司今天宣布,医生发起的4EVER临床研究全部120例患者队列已成功入组。随访设定在第1、第6和第12个月,即刻和6个月结果可望在2012年1月得出。
4EVER是一项前瞻性、非随机、多中心临床研究,评估SFA中Astron Pulsar和Pulsar-18支架的安全性和有效性。主要终点是第12个月的主要通畅度。两个次要终点分别是手术成功和创口并发症率。
4EVER的主要研究者、比利时Dendermonde的血管外科医生Dr. Marc Bosiers评论道:"4EVER研究的目的是展示Astron Pulsar和Pulsar-18支架植入最长达200毫米的SFA病灶中的有效性,其次是技术可行性和仅采用4F器械实施下肢介入的潜在安全性收益。若干研究已表明,在冠心病应用中,4F血管入路的创口并发症低于6F,预计4EVER将在外周应用中印证这些结果。"
BIOTRONIK公司血管介入部销售和营销副总裁Alain Aimonetti补充道:"越来越多的血管介入医生认识到4F介入的收益-不仅器械交叉较少、创口并发症降低,而且患者较早下床活动也有望节约成本、减少血管闭合器械的使用。"
BIOTRONIK公司近年来上市的4F导入器-套管兼容器械的阵容是业界最广泛的,这些器械旨在将对路的工具传递到外周血管介入医生的手中。此举将BIOTRONIK公司定位于血管器械创新的前沿-其亮点产品包括世界上首个完全兼容4F的200毫米自扩张支架Pulsar-18。
BIOTRONIK公司将为治疗下肢动脉疾病的医生不断驱动创新的微创解决方案 。2011年间,PTA阵容的进一步升级产品将上市,包括成功的Passeo-18 PTA序列中更长的球囊长度和基于0.014"的腘窝内专用PTA球囊Passeo-14。此外,Pulsar-18的优化支架设计将发布20-80毫米等不同长度规格,与前代器械相比,其径向力较高、灵活性甚至更大。
关于BIOTRONIK SE & Co. KG
BIOTRONIK公司是世界领先的心血管器械公司之一,已植入器械达数百万台,全球员工超过5600位,业务遍及100多个国家。BIOTRONIK公司密切感知医疗界的脉动、体味医生面临的挑战,从诊断、治疗到患者管理,为患者医护的所有阶段提供最佳解决方案。BIOTRONIK公司及其不断成功的理念在于品质、创新和临床卓越,从而为医生及其患者带来信心和安心。
更多信息请访问:www.biotronik.com。
发布时,请向我方提供副本。
图片/多媒体库,请访问: http://www.businesswire.com/cgi-bin/mmg.cgi?eid=6776015&lang=en
免责声明:本公告之原文版本乃官方授权版本。译文仅供方便了解之用,烦请参照原文,原文版本乃唯一具法律效力之版本。
联系方式:
BIOTRONIK SE & Co. KG
全球传播高级总监Sandy Hathaway
电话:+49 (0) 30 68905 1602
电子邮件:sandy.hathaway@biotronik.com
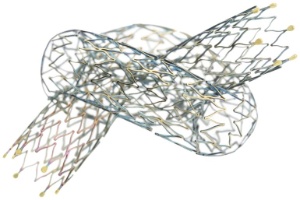
Astron Pulsar (照片:美国商业资讯)





