英格兰牛津--(美国商业资讯)--Exscientia plc (Nasdaq: EXAI)今天发布其EXS-21546 1期健康志愿者研究数据。EXS-21546是由Exscientia和Evotec SE(法兰克福证券交易所:EVT, MDAX/TecDAX,国际证券识别码:DE0005664809;纳斯达克股票代码:EVO)共同发明和开发的高选择性A2A受体拮抗剂。此项健康志愿者研究的顶线数据证实了Exscientia的靶标产品特性设计,包括效价、受体选择性高和预期的脑暴露量低以及未报告中枢神经系统不良事件,支持将EXS-21546推向高腺苷标志性实体瘤患者1b/2期研究。
此新闻稿包含多媒体内容。完整新闻稿可在以下网址查阅:https://www.businesswire.com/news/home/20220614005457/en/
Exscientia首席运营官兼药物发现主管David Hallett博士表示:“我们的EXS-21546 1a期研究的顶线数据显示,我们基于人工智能的平台能根据定义的设计目标来研制新型的分子,并具备人类生物学层面的高水平可转化性。EXS-21546是我们平台早期的试点项目。令我们自豪的是,它实现了我们在效价、选择性和药代动力学方面的目标。展望未来,A2AR拮抗剂临床开发的首要挑战是找出那些将最多受益于此类免疫调节治疗的患者。我们相信,利用我们独特的精准医学平台来分析患者的离体肿瘤微环境,包括免疫功能,将有助于我们为我们的药物识别出合适的患者。”
EXS-21546 1a期研究是三部分组成的剂量探索试验,评估EXS-21546单次递增剂量(SAD)和多次递增剂量(MAD)的安全性、耐受性、药代动力学(PK)和药效学(PD)。该研究将60名健康男性受试者随机分配到所有三个部分。该研究的主要目标之一是向癌症患者1b/2期研究提供EXS-21546的最佳起始剂量。
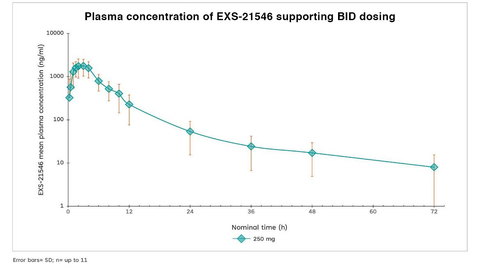
该研究显示,EXS-21546的人体PK观察结果与临床前模型所设计和预测的结果一致,支持每天两次(BID)剂量给药。EXS-21546在一个间隔内可持续抑制A2A受体。
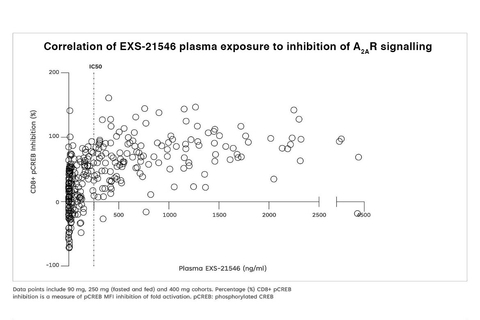
研究显示,EXS-21546在CD8阳性细胞中对CREB磷酸化有剂量依赖性抑制,PD特性可反映血浆暴露量。A2A受体信号传导的抑制作用在BID给药期间持续存在,展示出持久水平的靶点结合。
EXS-21546耐受良好,在所有剂量(30毫克、90毫克、250毫克、400毫克)的SAD部分和150毫克BID的MAD部分均未报告CNS不良事件。MAD阶段观察到1例受试者出现ALT和AST升高的实验室异常,被划分为3级严重不良事件。该事件在受试者完成14天治疗3天后观察到,并在未加医疗干预的情况下缓解。该受试者在治疗期间没有症状,用药期间未报告任何不良事件。
基于上述结果,Exscientia预计将在 2022 年下半年启动EXS-21546治疗高腺苷标志性实体瘤患者的1b/2期研究。此项1b/2期研究旨在评估较高剂量的EXS- 21546。
公司希望在未来的医学会议上分享此项1a期研究的追加数据。
关于EXS-21546
EXS-21546是Exscientia和Evotec基于人工智能共同发明和开发的A2A受体拮抗剂。Exscientia利用其人工智能驱动的平台设计出该化合物,而Evotec提供生物学和化学能力。
部分肿瘤可产生高水平的腺苷,它会结合并激活免疫细胞上的A2A受体,从而抑制免疫系统的抗肿瘤活性。研究正在评估EXS-21546能否防止高浓度的腺苷激活 A2A受体,从而促进免疫细胞的抗肿瘤活性。
关于EXS-21546 1a期试验
此项1期研究是针对男性健康志愿者的三部分研究,旨在评估EXS-21546的安全性、耐受性、药代动力学和药效学(PK/PD)。第1部分是一项随机、双盲、安慰剂对照、SAD研究并评估食物效应,41例健康志愿者以3:1比例随机分组(每个队列中,6例用活性药物,2例用安慰剂)。第2部分是为期14天的随机、双盲、安慰剂对照、MAD研究。第2部分在1个队列(8例受试者每天接受两次150毫克EXS-21546)入组后完成。第3部分是3向交叉、开放、随机研究,11例受试者入组后对照评估胶囊剂型(餐后和空腹)与口服混悬液(空腹)剂型。
关于Exscientia
Exscientia是一家人工智能驱动的制药公司,致力于以迅速而有效的方式发现、设计和开发尽可能优质的药物。Exscientia开发了首个功能性精准肿瘤学平台,在前瞻性介入临床研究中成功指导治疗选择和改善患者预后,同时将人工智能设计的小分子药物推向临床。我们的产品线彰显了我们将科学概念快速转化为精确设计的候选治疗药物的能力,目前已有超过30个项目正在推进。通过更快地设计更好的药物,我们相信至优科学理念能迅速成为患者的至优药物。
Exscientia总部位于牛津(英国英格兰),在维也纳(奥地利)、邓迪(英国苏格兰)、波士顿(美国马萨诸塞州)、迈阿密(美国佛罗里达州)、剑桥(英国英格兰)和大阪(日本)设有办事处。
请访问我们的网站:https://www.exscientia.ai,或者在Twitter上关注@exscientiaAI。
前瞻性陈述
本新闻稿包含1995年《私人证券诉讼改革法案》“安全港”条款所定义的某些前瞻性陈述,包括Exscientia 对候选分子开发进展以及对Exscientia 候选产品的临床前研究和临床试验的时间和进展及其报告的数据的期望的陈述,以及Exscientia 对其精准医疗平台和人工智能驱动的药物发现平台的期望的陈述。诸如“预期”、“相信”、“期望”、“打算”、“预测”、“预期”和“未来”等措辞或类似表述旨在识别前瞻性陈述。上述前瞻性陈述受制于预测未来结果和状况时所固有的不确定性之影响,包括Exscientia产品开发工作的范围、进展和扩展;Exscientia及其合作伙伴的临床试验的启动、范围和进展以及对其成本的影响;临床、科学、监管和技术发展;以及在发现、开发和商业化安全和有效的人类治疗候选产品的过程中,以及在围绕这些候选产品建立业务的工作中所固有的风险。除非法律要求,否则Exscientia没有义务公开更新或修改任何前瞻性陈述,无论是由于新信息、未来事件或其他原因。
原文版本可在businesswire.com上查阅:https://www.businesswire.com/news/home/20220614005457/en/
免责声明:本公告之原文版本乃官方授权版本。译文仅供方便了解之用,烦请参照原文,原文版本乃唯一具法律效力之版本。
联系方式:
投资者:
Sara Sherman
investors@exscientia.ai
媒体:
Amanda Galgay
media@exscientia.ai
(图示:美国商业资讯)
(图示:美国商业资讯)



